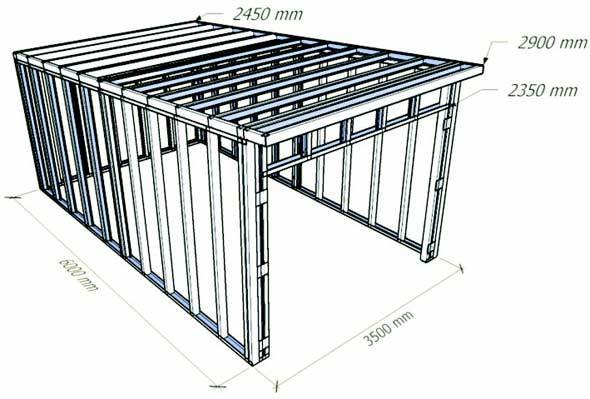
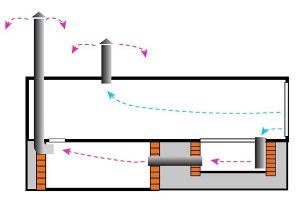
Способы защиты металлов от коррозии
Предотвращение начала или активного протекания коррозии – более удачный способ избавиться от проблем с разрушением металлов, чем постоянная замена или восстановление деталей. Поэтому все производители металлических изделий уделяют максимум внимания разработке и совершенствованию способов защиты своей продукции от ржавления.
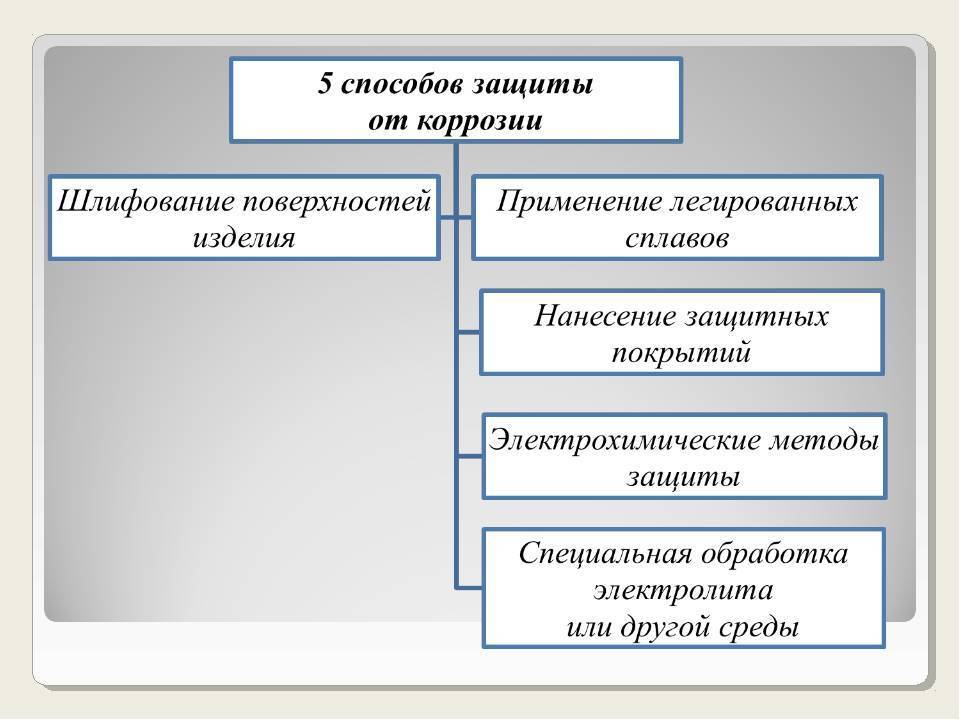
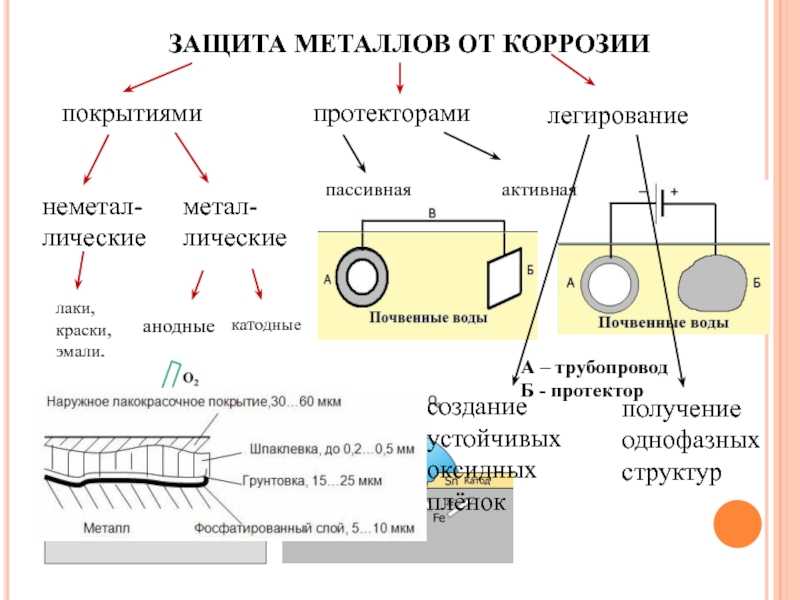
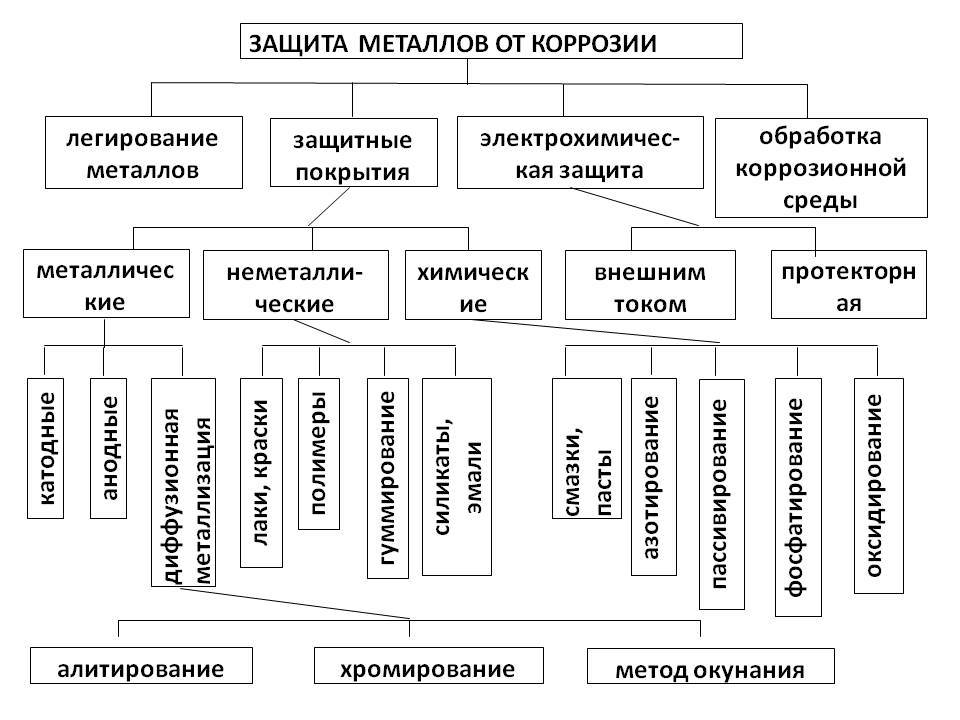
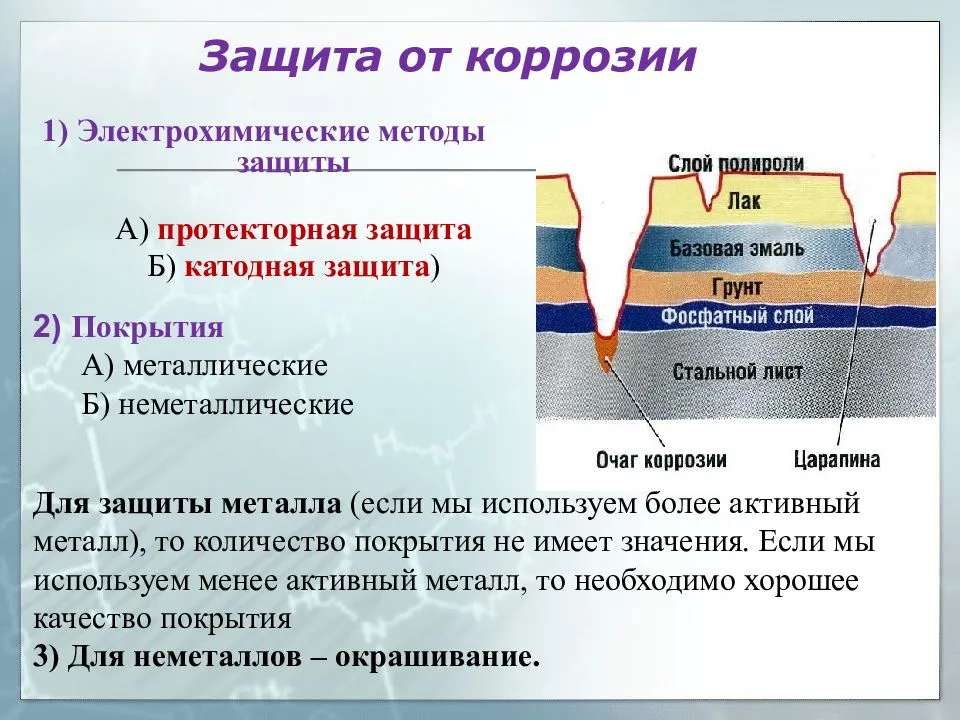
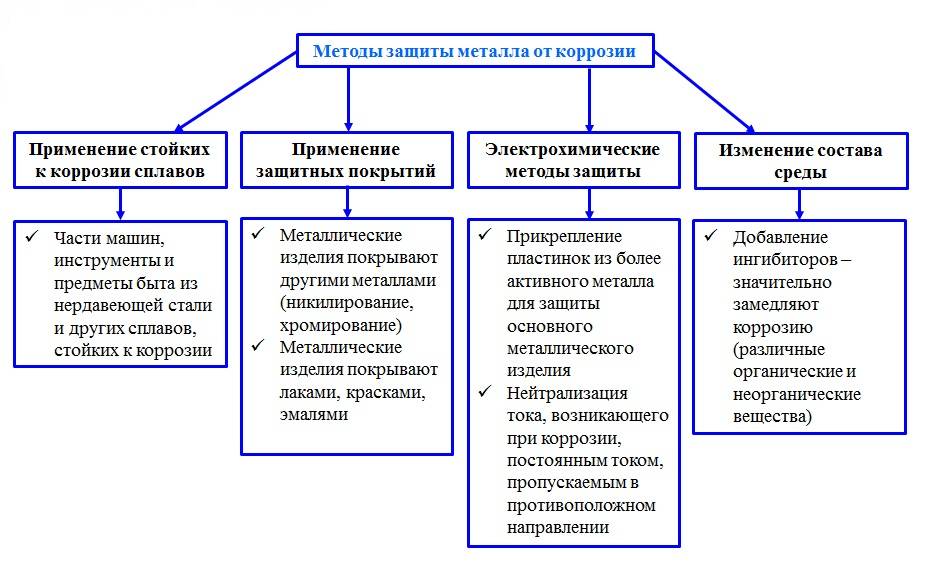
На данный момент есть четыре основных направления:
- изменение свойств металла введением добавок. По этому принципу изготавливаются нержавеющие стали – добавки хрома (12%) повышают стойкость сплава к коррозии до почти полной невосприимчивости в нормальных бытовых условиях. Изменения температуры и состава окружающей среды снижают стойкость нержавеющей стали к коррозии;
- использование защитных покрытий. Применяются различные (в чистом виде и комбинациях) лако-красочные, эмалевые, полимерные составы. Также – и с большим успехом – используется поверхностное нанесение менее активных химически металлов (оцинковывание, хромирование, никелирование, золочение);
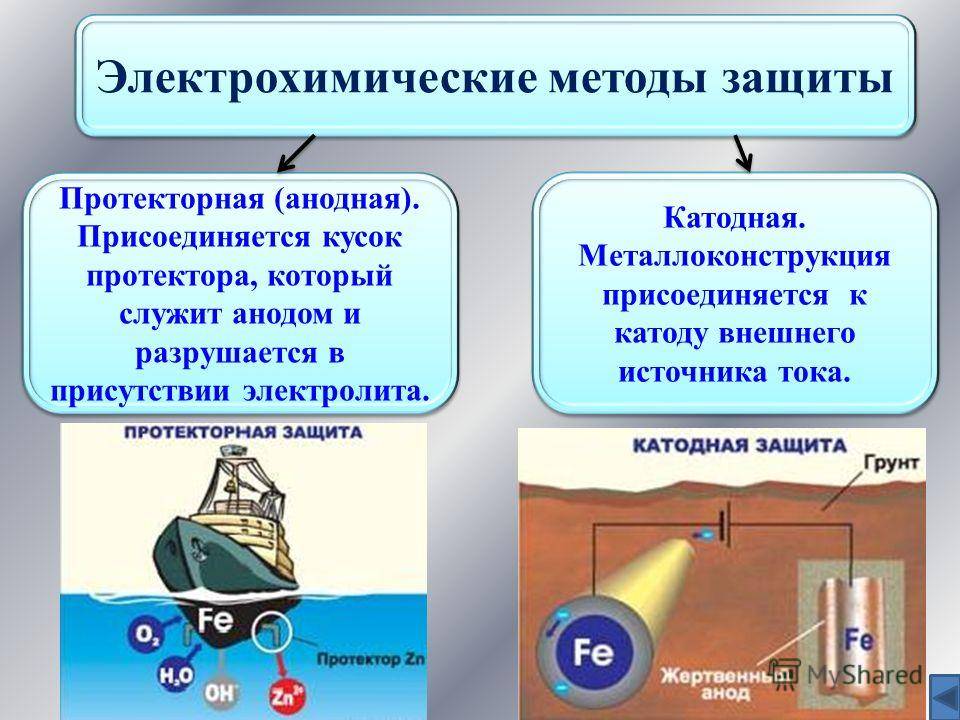
- применение небольших элементов (пластинок, заклепок) из более активных металлов для сохранения основного объема и массы изделия – коррозии в этом случае подвергаются именно добавленные элементы. Отдельно можно выделить создание слабого тока в самом изделии для нейтрализации тока электрохимической коррозии. Применение этого способа ограничено определенными условиями эксплуатации;
- введение ингибиторов – веществ, угнетающих процесс коррозии – в окружающую изделие среду.
Последний метод требует отдельного рассмотрения.
Характерные типы поражения ржавчиной
Способы защиты стали и сплавов зависят не только от вида коррозии, но и от типа разрушения:
- Ржавчина покрывает поверхность изделия сплошным слоем или отдельными участками.
- Выступает в виде пятен и точечно проникает вглубь детали.
- Разрушает металлическую молекулярную решетку в виде глубокой трещины.
- В стальном изделии, состоящем из сплавов, происходит разрушение одного из металлов.
- Более глубокое обширное ржавление, когда не только постепенно нарушается поверхность, но и происходит проникновение в глубокие слои конструкции.
Типы поражения могут быть комбинированные. Иногда их трудно определить сразу, особенно когда происходит точечное разрушение стали. Методы защиты от коррозии включают в себя специальную диагностику для определения степени повреждений.
Выделяют химическую коррозию без возникновения электрических токов. При соприкосновении с нефтепродуктами, спиртовыми растворами и другими агрессивными ингредиентами происходит химическая реакция, сопровождаемая газовыми выделениями и высокой температурой.
Электрохимическая коррозия — это когда металлическая поверхность контактирует с электролитом, в частности с водой из окружающей среды. В этом случае происходит диффузия металлов. Под воздействием электролита возникает электрический ток, происходит замещение и движение электронов металлов, которые входят в сплав. Структура разрушается, образуется ржавчина.

Выплавка стали и ее коррозионная защита – это две стороны одной медали. Коррозия наносит огромный вред промышленным и хозяйственным постройкам. В случаях с масштабными техническими сооружениями, к примеру, мостами, опорами электропередач, заградительными сооружениями, может спровоцировать и техногенные катастрофы.
Особенности антикоррозионных составов
 В местах скола краски видна ржавчина, а на осях покрытых смазкой коррозии нет
В местах скола краски видна ржавчина, а на осях покрытых смазкой коррозии нет
Что такое ингибиторы коррозии? Это такие вещества и элементы, которые, присутствуя в среде, подверженной опасному влиянию коррозии, в состоянии уменьшать и в целом останавливать коррозионное воздействие на металл. Ингибитор коррозии может представлять собой как одно химическое соединение, так и быть смесью многих.
Ингибиторами наиболее часто являются ПАВ вещества, а также всевозможная органика. При влиянии на изделие они еще сильнее улучшают защитные характеристики оксидной пленки на металле. По этой причине вы можете сделать вывод, что присутствие кислорода в среде благоприятствует подъему защитного эффекта от воздействия коррозии. Однако, если оксидная пленка имеет слабую устойчивость — ухудшается адсорбция ингибитора на верхнем слое металла.
- Ингибитор солеотложений ИОМС-1 (раствор)г 200 руб/кг. Макрофлекс.
- Ингибитор коррозии Protectogen(протектоген). C Aqua.
- Комплексонат – раствор цинкового комплекса. Эктоскейл.
- ГАЛАН. Протектор. Ингибитор коррозии (5 л). Защищает от коррозии трубопроводы, радиаторы и прочие системы отопления.
Как увеличить эффективность протекторов?
Чаще всего протекторные композиции применяются совместно с лакокрасочными составами, имеющими антикоррозийные свойства. Лакокрасочная защита самостоятельно не дает нужного эффекта, но при сочетании с протектором:
- позволяет устранить изъяны покрытия металлического сооружения, которые возникают в процессе эксплуатации (вспучивание, отслоение, набухание металла, появление трещин и пр.);
- снижает расход протекторных составов, увеличивая срок службы (при довольно высокой стоимости защитных сплавов это значимый эффект);
- обеспечивает равномерное распределение защитного тока по поверхности металлического трубопровода.
Конечно, на эксплуатируемое судно или резервуар нанести лакокрасочный состав довольно сложно. В этом случае лучше отказаться от его применения, а использовать только протекторы.
Бытовые и профессиональные способы справиться с ржавчиной. Что лучше?
Если правильно ухаживать за металлическими материалами, вовремя проводить диагностику и зачищать их, можно избежать разрушительного развития коррозии металла. Но если предмет, например, болт, уже сильно заржавел что делать?
«ЦНИИПСК КОРТЕСТ» в рамках программы телеканала РЕН ТВ провела эксперимент на качество вспомогательных смазок для откручивания. Для испытания были взяты несколько ржавых образцов. Сотрудник попытался выкрутить болт из гайки и замерил с помощью специального прибора – динамометра, сколько силы ему пришлось приложить к этому. Затем на этот же ржавый болт наносится средство и все действия повторяются вновь. Так было сделано с 4 средствами, сравним их:
- «Жидкий ключ» из автомагазина. Стоимость – 192 рубля. Сила воздействия на болт после нанесения снизилась на 12 Н*м.
- «Термоключ». Стоимость – 400. Болт стал откручиваться легче на 8 Н*м.
- Раствор своими руками из графитовой смазки (10-20мл), преобразователя ржавчины (30-40мл) и растворителя (150мл). Стоимость – 180р. Сопротивление снизилось на 8 Н*м.
- «Керосин». Стоимость 50р. После обработки очередного болта и гайки раскрутить их оказалось легче на 18 Н*м.
Таким образом, самое дешевое народное средство оказалось наиболее успешным для откручивания болтов с сильной коррозией. Оно обладает высокой проникающей способностью в отверстия, куда не может попасть вода. Поэтому поверхность металла полностью смазывается керосином.
И всё же самое лучшее и экономичное решение – не допускать губительного развития ржавления металла. Для этого стоит изначально использовать обработку защитными покрытиями и пользоваться услугами диагностики и защиты лаборатории «ЦНИИПСК КОРТЕСТ».
Бытовые антикоррозийные средства
Сегодня существует довольно много антикоррозийных составов, которые могут очень сильно отличаться по своей цене. Разница в стоимости объясняется прежде всего их долговечностью, надежностью и другими свойствами, которые обусловлены химическим составом. Если не учитывать небольшие различия в составах между разными средствами, то можно выделить не так уж и много типов антикоррозийных средств бытового назначения. При их выборе руководствуются не только составом, но и будущими условиями эксплуатации, что зачастую является самым важным факторов.
Классифицируют их по разному, например, краски делят по типу связывающей основы, где выделяют алкидные, эпоксидные и акриловые. Также они разделяются на две большие группы: обычные и термостойкие, которые способны выдерживать высокие температуры и не терять свои свойств. Также у них есть и другие параметры, такие как скорость высыхания, срок службы и т.д. Помимо красок можно выделить следующие группы антикоррозийных средств:
Пасты и смазки, которые производят на основе минеральных масел с добавлением воска или парафина. В зависимости от типа металла в них могут добавлять и другие вещества, например, в смазки для изделий из стали добавляют щелочь. Смазки и пасты используются преимущественно для защиты металлических изделий при их длительной транспортировки. Они обеспечивают отличную защиту, но для изделий из металла, которые эксплуатируются ежедневно они не подходят, так как их устойчивость даже к небольшим механическим воздействиям очень низкая.
Резиновые защитные антикоррозийные покрытия можно отнести как к промышленным, так и к бытовым. Суть в нанесении покрытия из эбонита или резины, которое может иметь совершенно разные характеристики. Например, широкий температурный диапазон эксплуатации, ее способность выдерживать нагрузки разных видов (растягивающие, ударные и т.д.), мягкость. Чаще всего подобные антикоррозийные покрытия делают еще на этапе производства.
Полимерные покрытия это достаточно большой класс, который сделан на основе полиэтилена, поливинилхлорида и других синтетических материалов. Как и в предыдущем случае, этот вариант используется чаще всего при производстве, но есть и бытовое применение.
В быту чаще всего приходится использовать лакокрасочные средства. Самыми распространенными являются алкидные эмали, в том числе и отечественного производства. Но сегодня подобные антикоррозийные составы выпускают даже в спреях, что является одним из самых удобных вариантов с точки зрения эксплуатации. Их легко наносить, можно создать равномерный слой и защитить даже самые труднодоступные местах.
Также стоит отметить, что для действительно надежной защиты используют не только собственно защитные покрытия, но и грунтовку, которая проникает в структуру металла и обеспечивает более внушительную защиту. Про них вы можете прочитать в этом материале, здесь же скажем, что использование грунтовок это всегда дополнительные расходы (а хорошие стоят дорого), но если нужно действительно надежно защитить металл, то их использование можно считать обязательным. Есть и средства для удаления ржавчины.
Типы коррозии и описание процесса
- Химическая — это такой тип взаимного влияния металла с окружающей средой, в процессе действия которого окисление и дальнейшее восстановление части среды проходят в едином акте. Продукты взаимного влияния не имеют разделения в пространстве.
- Электрохимическая — это такой тип взаимного влияния металла с коррозийным пространством, в котором реакция ионизации коррозионной среды проходит в нескольких актах.
- Газовая— это коррозия металлических поверхностей при слабом содержании воды (обычно влаги находится не больше 0,2 %) либо при максимальных рабочих температурах. В современной химической и газовой промышленности подобный тип коррозии может встречаться чаще остальных.
- Атмосферная — это тип коррозии в воздушной атмосфере либо в среде влажного газа.
- Биокоррозия — это биологический тип коррозии металла, который протекает под воздействием жизнедеятельности микробов и разных микроорганизмов.
- Контактная — это такой тип коррозии, который провоцируется контактом нескольких типов металлов с различными стационарными потенциалами.
- Радиационная — это такой тип коррозии металла, который обусловлен влиянием радиоактивного облучения.
Также существует коррозия внешним или блуждающим электрическим током. Еще один тип коррозии — это коррозия под напряжением, которая спровоцирована одномоментным влиянием коррозионной среды и протеканием механического напряжения
Важно учитывать, что данный тип коррозии является очень вредным, в особенности для систем, испытывающих сильные физические нагрузки
Виды коррозии металлов
Процесс коррозии – совокупность химических и электрических процессов, которые оказывают негативное воздействие на металл. В зависимости от типа воздействия коррозию классифицируют по нескольких признакам.
Коррозионные процессы различаются по:
Механизму реакций взаимодействия металла со средой:
а) химическое – процесс распада металла происходит в результате химической реакции с жидкостью, которая не проводит электрический ток или сухим газом.
Газовая коррозия возможна только в условиях высоких температур.
Например, если заводскую автомобильную выхлопную трубу заменить незащищенной стальной, то, когда машина заведется, начнется процесс ржавления, так как температура выхлопа составляет 500 ⁰С
б) электрохимическое – процесс, когда на металл действует электрический ток, либо электролит.
При взаимодействии электрического тока с металлом происходит процесс «выбивания» частиц последнего, в результате повреждается только та часть конструкции, которая была в контакте;
в) радиационное;
г) микробиологическое – процесс ржавления происходит в результате воздействия на металл агрессивных микроорганизмов. Данный вид коррозии характерен для подземных коммуникаций.
Но стоит отметить, что отходы жизнедеятельности птиц, также могут привести к началу процесса ржавления, так как в них содержится большое количество бактерий.
Виду коррозионной среды:
а) почвенная – характерна для трубопроводов, кабелей, опорных конструкций, то есть всего металла, который погружен в землю.
Основными характеристиками коррозионной активности почвы являются ее электропроводность, то есть способность проводить электрический ток, и влажность.
Наиболее активно проводят ток влажные, пористые грунты.
Например, если песок в сухом состоянии практически не проводит ток, то при увлажнении его на 2-3%, его проводимость увеличивается в 20 раз, а после высыхания возвращается в исходное состояние.
Для этого типа коррозионной среды характерны язвенные разрушения металла.
б) атмосферная – данный тип ржавления происходит при нахождении металлов на воздухе.
Быстрота протекания процесса коррозии зависит от типа климата и состава сплава.
В случае если влажность климата ниже 60% происходит сухая коррозия, то есть металл начинает окисляться.
Стоит отметить, что чем жарче климат, тем быстрее протекает сухая коррозия.
Если влажность выше 60%, то процесс разрешения металла происходит быстрее, так как влага проникает в микротрещины и зазоры, что приводит к образованию окисей.
в) морская – самый опасный тип коррозии.
В морской воде ржавление металла происходит под воздействием солей, микроорганизмов и большого количества кислорода, что приводит к быстрому разрушению большинства сплавов.
Стоит отметить, что процесс разрушения будет проходить интенсивнее выше ватерлинии, так как там происходит периодический контакт с водой;
3) Характеру дополнительных воздействий:
а) коррозионное растрескивание – ржавление, которое развивается в местах, стороннего воздействия на металл тяжелых весов;
б) эрозионная коррозия – разрушение, которое происходит при трении в условиях агрессивной среды;
в) кавитационная коррозия – разрушение, которое происходит при ударных воздействиях в условиях агрессивной среды.
Защита от коррозии в промышленности и быту
Необходимо обеспечить металлу надежную защиту от коррозии. Все условия, когда требуется защита металлов от коррозии, кратко можно поделить на промышленные и бытовые.
В промышленности существует несколько вариантов антикоррозийной защиты:
- Пассивация. В процессе производства в сталь добавляются другие металлические сплавы (молибден, никель, ниобий). Эти материалы характеризуются отличными эксплуатационными свойствами и высокой стойкостью к агрессивным воздействиям. Эти разновидности стали принято называть легированными.
- Нанесение на поверхность стали каких-то других металлов. При этом на изделии образуется защитное покрытие. Зачастую для данной цели применяется алюминий, кобальт и хром.
- Применение специальных протекторов и анодов. При контакте детали с водой происходит разрушение протектора, который образует защитное покрытие. Такая методика часто используется в производстве деталей для морских буровых установок и судов.
Промышленные способы обеспечения антикоррозийной защиты очень разнообразны. К ним относится и покрытие специальной стекловолоконной эмалью, и химическая защита, и многие другие.
Антикоррозийная защита материала в домашних условиях подразумевает применение ЛКМ-покрытий и химических средств. Свойства защитного плана обеспечивают сочетанием разных элементов: смол на основе силикона, ингибиторов, полимеров, металлической стружки и пудры.
Следует отметить, что перед окрашиванием детали, ее нужно обработать специальным преобразователем коррозии или грунтовкой, иначе ее эксплуатационные свойства будут быстро уменьшаться.
Сегодня в продаже встречается несколько разновидностей преобразователей ржавчины:
- Средства-грунтовки. Характеризуются высокой адгезией с металлическими поверхностями, способствуют выравниванию покрытия перед покраской. Во многих грунтовках содержатся ингибиторы, тормозящие коррозийные процессы. Кроме того, заблаговременное нанесение слоя грунтовки позволяет сэкономить на окрашивании.
- Химические препараты. Преобразуют окись железа в более безопасные вещества, которым не страшна коррозия. Такие средства называются стабилизаторами.
- Составы, преобразующие ржавчину в обычные соли.
- Масла и смолы, уплотняющие и связывающие ржавчину, обеспечивая ее нейтрализацию.
Специалисты советуют подбирать краску и грунтовку какого-то одного производителя, чтобы их химический состав не имел особых отличий.
Таблица 1. Совместимость металлов
| Металлы, в отношении которых представлены данные в таблице по подверженности их коррозии | Соотношение площади металла к другим металлам таблицы | Магний | Цинк | Алюминий | Кадмий | Свинец | Олово | Медь |
|---|---|---|---|---|---|---|---|---|
| Магний | Низкое | С | С | С | С | С | С | |
| Высокое | У | У | У | С | С | |||
| Цинк | Низкое | У | У | У | С | С | С | |
| Высокое | Н | Н | Н | Н | Н | Н | ||
| Алюминий | Низкое | У | Н | Н | С | С | ||
| Высокое | Н | У | Н | С | С | С | ||
| Кадмий | Низкое | Н | Н | Н | С | С | С | |
| Высокое | У | Н | Н | Н | Н | Н | ||
| Углеродистая сталь | Низкое | Н | Н | Н | Н | С | С | С |
| Высокое | Н | Н | Н | Н | Н | Н | Н | |
| Низколегированная сталь | Низкое | Н | Н | Н | Н | С | С | С |
| Высокое | Н | Н | Н | Н | Н | Н | Н | |
| Литейная сталь | Низкое | Н | Н | Н | Н | С | С | С |
| Высокое | Н | Н | Н | Н | Н | Н | ||
| Хромированная сталь | Низкое | Н | Н | Н | Н | У | У | С |
| Высокое | Н | Н | Н | Н | Н | Н | ||
| Свинец | Низкое | Н | Н | Н | Н | Н | Н | |
| Высокое | Н | Н | Н | Н | Н | |||
| Олово | Низкое | Н | Н | Н | Н | Н | ||
| Высокое | Н | Н | Н | Н | Н | |||
| Медь | Низкое | Н | Н | Н | Н | У | С | |
| Высокое | Н | Н | Н | Н | Н | У | ||
| Нержавеющая сталь | Низкое | Н | Н | Н | Н | Н | Н | |
| Высокое | Н | Н | Н | Н | У | У | Н | |
В 1 столбце таблицы представлены металлы, которые подвергаются или не подвергаются коррозии с металлами указанными в остальных столбцах таблицы и пропорция соотношения площадей металла, указанного в 1 столбце, к металлам в остальных столбцах таблицы. Краткое обозначение С, У, Н в таблице означает:
|
Способы защиты металлов от коррозии
Полностью избежать коррозии вряд ли удастся, однако можно существенно замедлить ее проявление. Достигается это путем изменения свойств металла и/или среды либо создания преграды между ними.
Антикоррозийные покрытия
Антикоррозийные покрытия предполагают создание изолирующего слоя, препятствующего контакту активных элементов металла и окружающей среды. Различаются по составу и технологии нанесения.
Неметаллические антикоррозийные покрытия.
- Лакокрасочные покрытия. Наносится на поверхность металлических изделий, образуя при высыхания защитную пленку. Имеют в свои составе различные вещества, формирующие стойкость к определенным воздействиям. Термостойкие эмали предназначены для эксплуатации под воздействием высоких температур, сохраняют защитные свойства и пожаробезопасность при сильном нагреве. Эмали с гидрозащитой на основе полиуретана предохраняют от контактов с водой и механических повреждений. Срок службы до 5 лет.
- Полимерные покрытия. Антикоррозийные покрытия на основе полимеров наносится на тщательно очищенную поверхность изделия в виде горячей смолы. После остывания образуют плотную пленку толщиной до двух миллиметров, обеспечивающую надежную защиту в течение 10 лет и более.
- Резиновые покрытия. Являются надежным диэлектриком, обеспечивают механическую защиту. Наносятся на очищенную и обработанную резиновым клеем поверхность с последующим процессом вулканизации. Могут быть твёрдыми или мягкими в зависимости от количества серы в составе резины.
- Силикатные порошковые покрытия. Устойчивы к воздействию агрессивных сред, давления, высоких температур. Создаются в несколько этапов. Порошкообразная эмаль наносится на подготовленную металлическую поверхность, затем запекается при 180 — 220 градусах. Для получения нескольких слоев операции повторяются.
- Пасты и смазки изготавливаются на основе минеральных масел и восков. При высыхании образуют защитную пленку, чувствительную к механическим воздействиям. Применяются для защиты металлоизделий при хранении.
Металлические покрытия
Защита металла от коррозии с помощью другого металла выступает оптимальным способом обработки при электрохимической коррозии. Защитный металл должен иметь отрицательный потенциал в создающейся гальванической паре, играя роль анода. Тогда именно он будет вступать в реакцию со средой, тем самым ограждая базовый металл изделия от разрушения. Процесс создания анодного покрытия называется анодированием.
Для анодирования широко применяемой в промышленности стали чаще всего используется цинк. Он обеспечивает электрохимическую защиту, устойчив к механическим воздействиям и экономичен по стоимости. Его наносят различными способами.
- Горячее цинкование — погружение детали в расплавленный цинк.
- Гальваническое цинкование — обработка в гальванической ванне, когда цинк оседает на поверхности стали под действием электрического тока.
- Газо-термическое цинкование — напыление расплавленного цинка с помощью воздушной струи.
- Термодиффузионное цинкование — воздействие высокой температуры для проникновения цинка в поверхностный слой обрабатываемого металла.
- Холодное цинкование — нанесение цинкосодержащего состава методом покраски, с помощью кисти, валика или распылителя.
Легирование металла
Укрепление защитных свойств самого металла происходит за счет удаления из него компонентов, ускоряющих коррозионные процессы, либо введения примесей, замедляющих их. Проводится на этапе производства металла, а также при механической или термической обработке деталей. Наиболее известным легированным сплавом является нержавеющая сталь, получаемая путем добавочного внедрения хрома и никеля.
Изменение состава среды.
Выполняется посредством введения в пространство, окружающее металлоизделия, специальных веществ, замедляющих коррозионные процессы — ингибиторов. Ингибиторы адсорбируются на поверхности металла, за счет чего приостанавливается процесс коррозии.
Другой вариант — удаление из состава среды агрессивных компонентов. Для этого может проводиться, к примеру, осушение воздуха и очистка его от примесей, вакуумирование (для сравнительно небольших объектов), работа в среде инертных газов (аргон, неон, ксенон). Данный метод требует дополнительного оборудования, используется главным образом в лабораториях и опытных производствах.
Активная электрохимическая защита.
Осуществляется путем наложения внешнего тока. Используется в ходе эксплуатации металлических конструкций с помощью специальных установок. Протекание постоянного электрического тока удерживает элементы металла и среды от взаимодействия и замедляет процесс коррозии.
Коррозия металла и способы защиты от нее
Ученые и инженеры разработали множество способов защиты металлических конструкций от коррозии.
Промышленные
Промышленные методы защиты металлических изделий подразделяются на ряд направлений:
- Пассивация. При выплавке стали в ее состав добавляют легирующие присадки, такие, как Cr, Mo, Nb, Ni. Они способствуют образованию на поверхности детали прочной и химически стойкой пленки окислов, препятствующей доступу агрессивных газов и жидкостей к железу.
- Защитное металлическое покрытие. На поверхность изделия наносят тонкий слой другого металлического элемента — Zn , Al, Co и др. Этот слой защищает железо о т ржавления.
- Электрозащита. Рядом с защищаемой деталью размещают пластины из другого металлического элемента или сплава, так называемые аноды. Токи в электролите текут через эти пластины, а не через деталь. Так защищают подводные детали морского транспорта и буровых платформ.
- Ингибиторы. Специальные вещества, замедляющие или вовсе останавливающие химические реакции.
- Защитное лакокрасочное покрытие.
- Термообработка.
 Способы защиты от коррозии, используемые в индустрии, весьма разнообразны. Выбор конкретного метода борьбы с коррозией зависит от условий эксплуатации защищаемой конструкции.
Способы защиты от коррозии, используемые в индустрии, весьма разнообразны. Выбор конкретного метода борьбы с коррозией зависит от условий эксплуатации защищаемой конструкции.
Бытовые
Бытовые методы защиты металлов от коррозии сводятся, как правило, к нанесению защитных лакокрасочных покрытий. Состав их может быть самый разнообразный, включая:
- силиконовые смолы;
- полимерные материалы;
- ингибиторы;
- мелкие металлические опилки.
Отдельной группой стоят преобразователи ржавчины – составы, которые наносят на уже затронутые коррозией конструкции. Они восстанавливают железо из окислов и предотвращают повторную коррозию. Преобразователи делятся на следующие виды:
- Грунты. Наносятся на зачищенную поверхность, обладают высокой адгезией. Содержат в своем составе ингибирующие вещества, позволяют экономить финишную краску.
- Стабилизаторы. Преобразуют оксиды железа в другие вещества.
- Преобразователи оксидов железа в соли.
- Масла и смолы, обволакивающие частички ржавчины и нейтрализующие ее.
 При выборе грунта и краски лучше брать их от одного производителя. Так вы избежите проблем совместимости лакокрасочных материалов.
При выборе грунта и краски лучше брать их от одного производителя. Так вы избежите проблем совместимости лакокрасочных материалов.
Методы противостояния коррозионным процессам
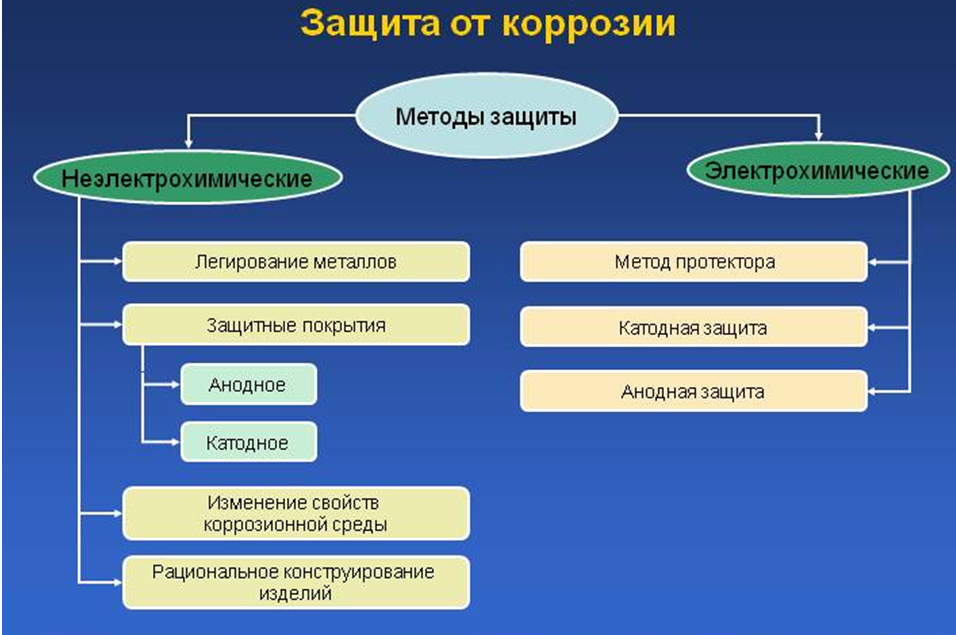
Основные методы, применяемые для противодействия коррозии, приведены ниже:
- повышение способности материалов противостоять окислению за счет изменения его химического состава;
- изоляция защищаемой поверхности от контакта с активными средами;
- снижение активности окружающей изделие среды;
- электрохимические.
Первые две группы способов применяются во время изготовления конструкции, а вторые – во время эксплуатации.
Методы повышения сопротивляемости
В состав сплава добавляют элементы, повышающие его коррозионную устойчивость. Такие стали называют нержавеющими. Они не требуют дополнительных покрытий и отличаются эстетичным внешним видом. В качестве добавок применяют никель, хром, медь, марганец, кобальт в определенных пропорциях.  Стойкость материалов к ржавлению повышают также, удаляя их состава ускоряющие коррозию компоненты, как, например, кислород и серу – из стальных сплавов, а железо – из магниевых и алюминиевых.
Стойкость материалов к ржавлению повышают также, удаляя их состава ускоряющие коррозию компоненты, как, например, кислород и серу – из стальных сплавов, а железо – из магниевых и алюминиевых.
Снижение агрессивности внешней среды и электрохимическая защита
С целью подавления процессов окисления во внешнюю среду добавляют особые составы – ингибиторы. Они замедляют химические реакции в десятки и сотни раз. Электрохимические способы сводятся к изменению электрохимического потенциала материала путем пропускания электрического тока. В результате коррозионные процессы сильно замедляются или даже вовсе прекращаются.
Пленочная защита
Защитная пленка препятствует доступу молекул активных веществ к молекулам металла и таким образом предотвращают коррозионные явления. Пленки образуются из лакокрасочных материалов, пластмассы и смолы. Лакокрасочные покрытия недороги и удобны в нанесении. Ими покрывают изделие в несколько слоев. Под краску наносят слой грунта, улучшающего сцепление с поверхностью и позволяющего экономить более дорогую краску. Служат такие покрытия от 5 до 10 лет. В качестве грунта иногда применяют смесь фосфатов марганца и железа.
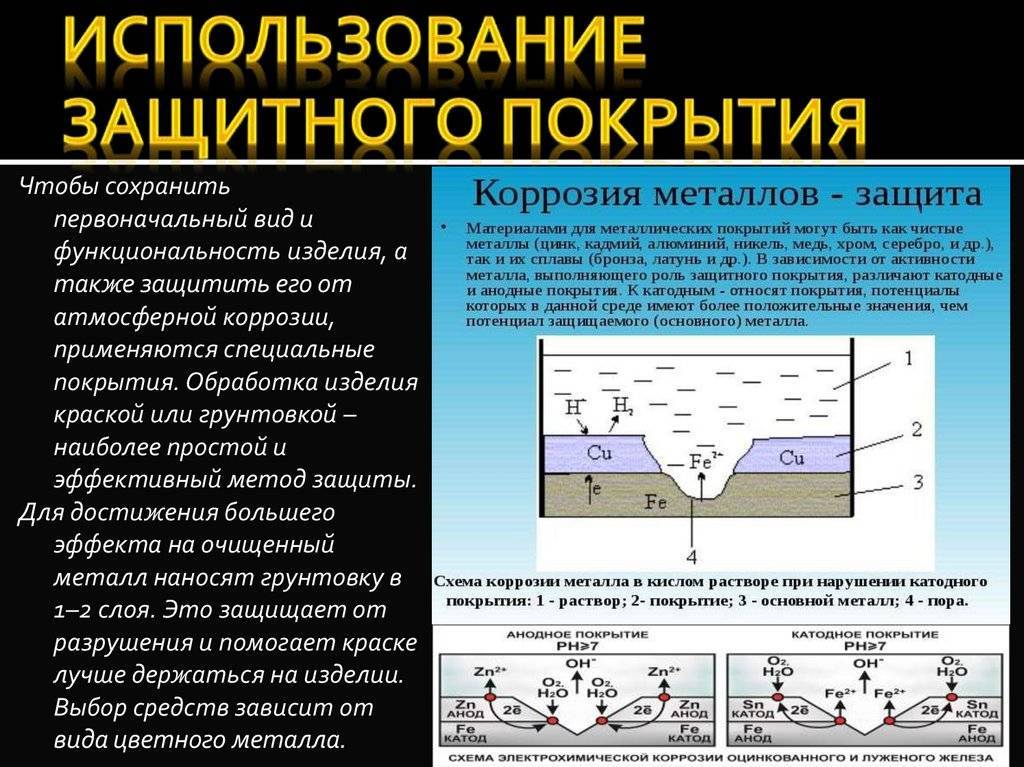
Защитные покрытия создают также из тонких слоев других металлов: цинка, хрома, никеля. Их наносят гальваническим способом. Покрытие металлом с более высоким электрохимическим потенциалом, чем у основного материала, называется анодным. Оно продолжает защищать основной материал, отвлекая активные окислители на себя, даже в случае частичного разрушения. Покрытия с более низким потенциалом называют катодными. В случае нарушения такого покрытия оно ускоряет коррозию за счет электрохимических процессов. Металлическое покрытие также можно наносить также методом распыления в струе плазмы. Применяется также и совместный прокат нагретых до температуры пластичности листов основного и защищающего металла. Под давлением происходит взаимная диффузия молекул элементов в кристаллические решетки друг друга и образование биметаллического материала. Этот метод называют плакированием.
Виды коррозии металлов
Учитывая сложность процесса и его многообразие, классификация видов коррозии ведется по нескольким группам признаков:
- механизм – химический или электрохимический;
- окружающая среда. Выделяют общую газовую, атмосферную (с наиболее активным действием кислорода), электролитную и неэлектролитную, подземную (иначе почвенную), биологическую среды. Также агрессивной средой считаются блуждающие токи;
- условия протекания. С погружением, без погружения и частичным погружением в среду, с непосредственным контактом, через щель, в результате трения. Выделяют межкристаллитное воздействие (по границам кристаллов и зон), коррозию под постоянным или переменным электрическим напряжением;
- степень разрушения объекта. Коррозия может быть сплошной, захватывающей всю поверхность объекта (равномерной, неравномерной, избирательной) или локальной. В этом случае отмечают пятна, язвы, точки и сквозные поражения, а также межкристаллитный вариант.
Несколько примеров для лучшего понимания сути и разновидностей коррозии.
- Повреждение днища автомобиля. Считается химическим, с активным действием влаги и атмосферного кислорода, активных газов выхлопа, дорожной «химии» и частично моющих средств при помывке авто. В случае пробоя электропроводки на днище могут воздействовать слабые токи, в этом случае коррозия будет уже электрохимической и заметно ускорится.
- Ржавление гвоздей и другого крепежа из сплавов железа в строительных конструкциях. Химический процесс, связан с атмосферной влагой и кислородом. При повышенной кислотности материала, в котором установлен крепеж, или увеличении кислотности атмосферных осадков и газовой среды ржавление усиливается и проходит быстрее.
- Сваи в морской воде. Активное воздействие агрессивного электролита (которым является морская вода) приводит к быстрому разрушению металлических конструкций. Скорость коррозии усиливают перепады температуры и механическое воздействие волн.
- Поверхностное разрушение сантехнических устройств и радиаторов отопления. Это характерный пример электрохимической коррозии, где в роли электролита выступает водопроводная вода (теплоноситель в отопительной системе) и моющие средства для сантехники.
Последний вариант (на фото) – это именно коррозия, но не ржавление, поскольку сплав, как правило, создается не на основе железа.